


2025年,FDA共批准46款新药 [1],包含34款新分子实体,其中30款为小分子新药。从给药途径和剂型来看,在这30款获批的小分子新药中,3款为液体制剂(其中包括2款滴眼液,1款鼻喷雾剂),27款为固体/半固体制剂(其中包括1款冻干粉针剂,1款乳膏剂),如下表1。
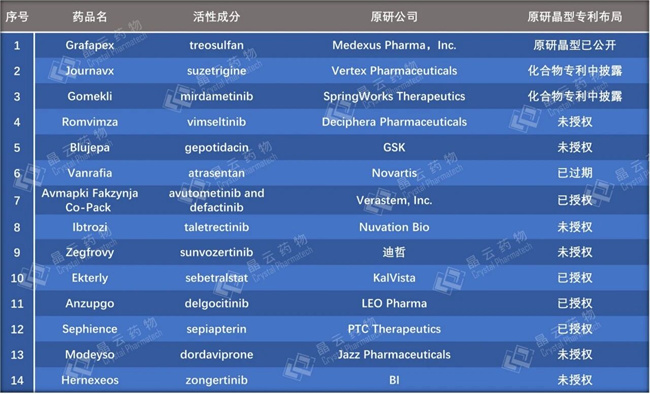
表1. 2025年FDA批准的34款新分子实体基本信息



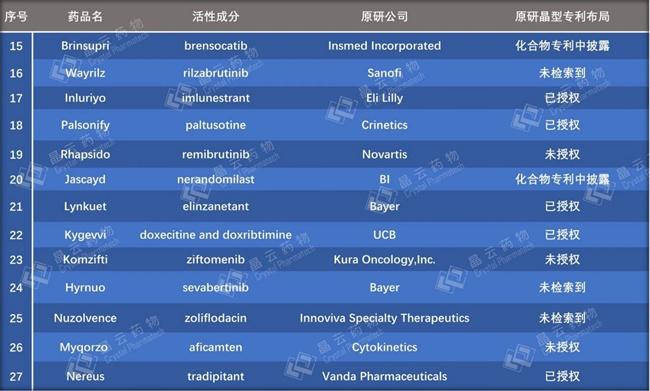
通过对27款固体/半固体制剂小分子新药的原研公司专利布局分析发现,共有22款产品已经布局了晶型专利(统计包括正在审查中的专利),占所有固体制剂/半固体制剂小分子新药的81.5%,具体信息见表2。
表2. 2025年FDA批准的27款固体/半固体制剂小分子新药的基本信息及晶型专利布局
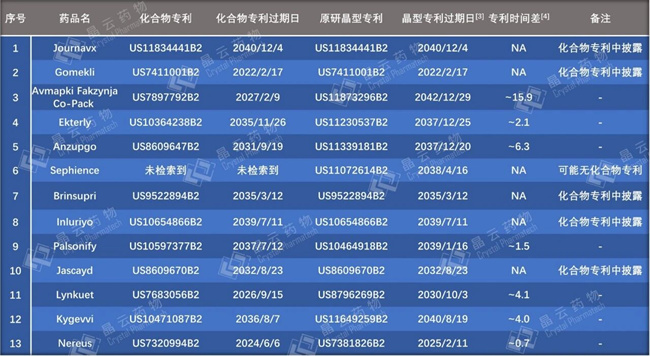
针对上述22款原研已有晶型专利布局的小分子新药,我们进一步分析了其化合物专利和晶型专利过期日及二者的时间差,结果见表3。未统计原研晶型专利还处于审查阶段的9个品种。有5个品种(Journavx、Gomekli、Brinsupri、Inluriyo、Jascayd)晶型相关信息已在化合物专利中被披露,另外8款品种原研晶型专利过期日均晚于化合物专利过期日,其中,时间差在3年(含3年)以上的有4个品种,时间差在5年(含5年)以上的有2个品种。
表3. 13个小分子新药的化合物专利和晶型专利分析
小编从上述13个品种中选取2个品种作为代表,进行详细介绍,以帮助读者更好理解创新药公司如何通过晶型专利布局延长产品生命周期。这2个品种的获批也极具里程碑式的意义,无论是从治疗疾病本身还是市场份额预估,都是集极具潜力的重磅品种。
Gomekli
GOMEKLI™(Mirdametinib)由SpringWorks Therapeutics研发,用于治疗年龄不低于2岁的1型神经纤维瘤病相关丛状神经纤维瘤(NF1-PN)成人和儿童患者。Mirdametinib是首个获批可同时用于治疗成人和儿童NF1-PN的药物,有望成为儿童NF1-PN患者的“best-in-class”疗法。Mirdametinib 是一种丝裂原活化蛋白激酶(MAP2K、MEK、MAPKK)抑制剂,可抑制 MEK1 和 MEK2 的激酶活性以及 ERK 的下游磷酸化。2025 年 2 月 11 日,Mirdametinib 获得 FDA 批准。
Mirdametinib的化合物专利(US7411001B2)于2022年2月17日过期,并在该篇专利中公开了两个晶型Form I和Form II。后续提交的晶型专利US11066358B1和US11084780B1披露了该化合物的更多晶型,过期日为2041年2月17日。尽管后续晶型专利与化合物专利过期日之间相隔了长达19年的时间,但化合物专利中披露的晶型仍然为仿制药的开发留下了一定空间。
Sephience
SEPHIENCE™ (Sepiapterin)是由PTC Therapeutics开发的用于治疗1月龄及以上且对Sepiapterin治疗有反应的成人和儿童高苯丙氨酸血症 (HPA) 患者的口服散剂。这是全球首款通过激活苯丙氨酸羟化酶 (PAH) 关键辅助因子BH4通路治疗PKU的口服疗法。Sepiapterin为四氢生物蝶呤(BH4)的天然前体,能激活苯丙氨酸羟化酶(PAH),同时通过独立的药理学伴侣作用,纠正PAH错误折叠以增强酶的功能。2025年7月28日,Botanix公司宣布美国FDA已批准Sofdra上市。
根据专利检索结果,推测Sepiapterin可能无化合物专利。其晶型专利US11072614B2保护了Sepiapterin游离碱的A/B/C/D/E/F/G晶型以及多种盐的晶型,过期日为2038年4月16日。原研公司在该药物晶型专利上的布局使得该药物在上市后仍有近13年的专利保护期。
总结
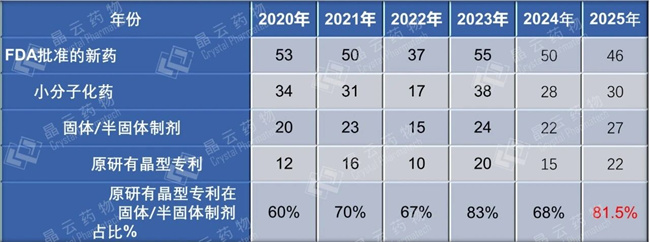
回顾近6年的数据(表4),虽然小分子化药获批的个数与去年基本持平,且固体/半固体制剂的小分子新药比例有所上升。近年来原研进行晶型专利布局的品种比例稳定维持在60%-85%的较高水平,新药开发过程中药物晶型专利布局的重要程度。一方面,晶型专利为核心化合物提供了关键的延伸保护与市场独占期拓展。当化合物专利到期后,优化的晶型专利能有效构筑后续防线,延长产品的市场独占权,保障研发回报。另一方面,特定晶型往往直接关联药物的稳定性和生物利用度等关键性能,其专利保护不仅覆盖物质形态本身,还常与制剂工艺和临床应用优势紧密结合,形成技术壁垒。因此,系统性的晶型研发与布局,既是完善知识产权保护网络、最大化商业价值的核心策略,也是通过技术迭代提升产品疗效与安全性的重要研发路径。
表4. 近6年FDA批准新药的晶型专利保护情况
参考文献及标注
[1] https://www.fda.gov/drugs/novel-drug-approvals-fda/novel-drug-approvals-2025.
[2] 化合物专利过期日以橙皮书记载的过期日为准:https://www.accessdata.fda.gov/scripts/cder/ob/index.cfm.
[3] 对于已授权专利,以官方公布的过期日为准。
[4] 晶型专利过期日减化合物专利过期日。
CRO事业部-撰稿人:
Yuhao、Jing 、Linlin、Ruonan