MOLECULE - MATERIAL - MEDICINE
资源中心
-
2026-05-21苏州•加拿大
跨越山海,共赴新程!很荣幸作为苏州生物医药产业的代表企业被提及。自2018年晶云药物加拿大子公司成立以来,我们一直致力于将全球顶尖的制剂技术与中国创新药研发深度融合。未来,晶云将继续发挥全球布局优势,做中国创新药走向世界的坚实桥梁。
-
2026-04-17战略合作 | 晶云药物成为亚太地区首家部署专用MicroED平台的企业,携手ELDICO Scientific AG深化战略合作
晶云药物(Crystal Pharmatech)是一家专注于药物晶型研究、临床前处方研究及小分子药物制剂开发及生产的科学驱动型CRO/CDMO企业,在中国、美国及加拿大设有全球研发与生产基地,为全球客户提供专业化服务。
-
2026-03-31【喜报】晶云药物全新高活性实验室正式启用!
近日,苏州晶云药物科技股份有限公司(以下简称“晶云药物”)位于苏州工业园区晶云大厦的OEB4/OEB5高活性实验室已全面建设完成,设备暴露控制能力成功通过第三方监测机构测试,将于即日起正式投入使用。这标志着晶云药物在高活性药物研发领域的硬件设施与安全管控能力迈上了全新台阶,能够为客户提供更安全、更高效、更专业的一站式研发服务。
-
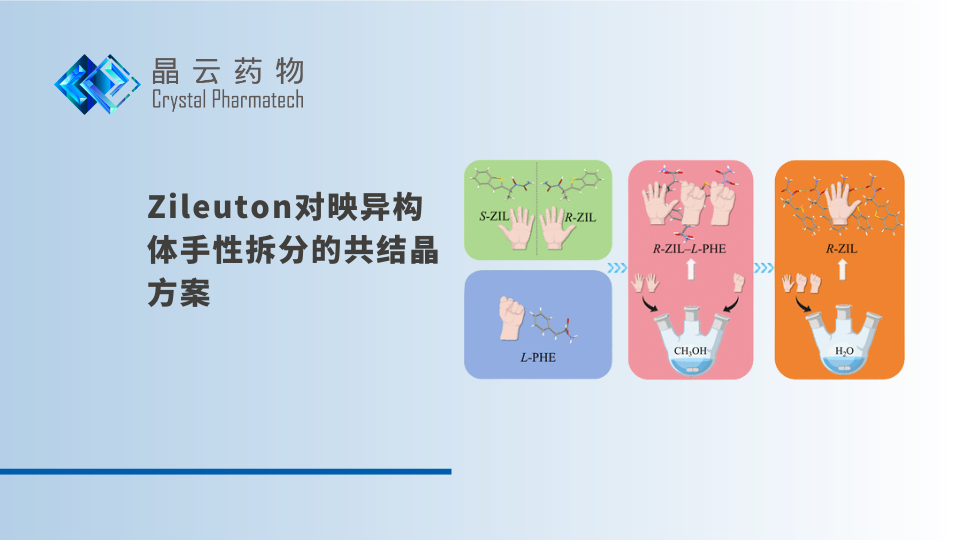
2026-03-25学术发表 | 晶体工程助力手性切换:Zileuton对映异构体手性拆分的共结晶方案
近日,由知名药物晶体工程专家张海禄博士担任通讯作者,晶云药物等多单位科研人员共同完成的学术论文
-
2026-03-17患者不想背冰箱出门?当博士研究直面真实世界
从西交利物浦大学到苏州生物医药产业园(BioBAY),有三公里左右的距离。读博四年间,王帅经常在这条路上往返。
-
2026-03-02【晶云•助力】晶云药物助力济煜医药1类创新药济乐美上市